Los elementos químicos en el Universo
En el Universo se han detectado alrededor de 90 elementos químicos distintos. La abundancia de cada uno de ellos es muy diferente, el hidrógeno constituye casi el 75% de la materia atómica del Universo, de un elemento como el francio apenas si existen 30 g en toda la Tierra, de otros elementos no se conoce su existencia y se han sintetizado en el laboratorio, en algunos casos, apenas unos pocos átomos. Este capítulo lo vamos a dedicar a conocer como el hombre ha ampliado, sintetizándolos de manera artificial, el número de elementos químicos conocido hasta llegar en la actualidad al 118, de ellos 112 reconocidos y con nombre admitido por la IUPAC.
Las estrellas, su
evolución y muerte: La gran cocina de los elementos
químicos
En el Universo primigenio y según cuenta la Teoría del Big-bang, solamente existían las partículas fundamentales. En unos 300000 años (muy poco tiempo si se tiene en cuenta la edad estimada del Universo, de unos 14000 millones de años) se habían formado los primeros átomos. Casi toda la materia formada era hidrógeno (un protón y un electrón), algo de deuterio (un protón, un neutrón y un electrón) y casi nada de helio (dos protones, dos neutrones y dos electrones). En algunos puntos del Universo donde la concentración de hidrógeno era mayor, éste se empezó a condensar debido a la fuerza de la gravedad, apareciendo las primeras estrellas y en su conjunto, las primeras galaxias. Aquí empezó a gestarse la inmensa fábrica de elementos que es una estrella.
Una estrella es una ingente masa de plasma (gas formado por iones y electrones a temperaturas muy altas) que se mantiene en equilibrio. Por un lado, la atracción gravitatoria haría que la estrella colapsara, pero por otro lado, la enorme presión que ejerce la estrella hacia su interior hace que la temperatura aumente hasta unos valores de millones de grados en su interior. A esa temperturas los átomos alcanzan unas velocidades enormes y al chocar entre si, se producen reacciones de fusión nuclear. En una reacción de este tipo, dos átomos se fusionan (deberíamos decir sus núcleos) y forman otro átomo distinto. Lógico, porque ha variado el número de protones del núcleo Por ejemplo, a partir del hidrógeno (protón) se puede obtener helio por el proceso denominado PP (protón-protón) y que se desarrolla en tres pasos:
1H +1H → 2H + e++ ν0
2H
+1H → 3HeEn el Universo primigenio y según cuenta la Teoría del Big-bang, solamente existían las partículas fundamentales. En unos 300000 años (muy poco tiempo si se tiene en cuenta la edad estimada del Universo, de unos 14000 millones de años) se habían formado los primeros átomos. Casi toda la materia formada era hidrógeno (un protón y un electrón), algo de deuterio (un protón, un neutrón y un electrón) y casi nada de helio (dos protones, dos neutrones y dos electrones). En algunos puntos del Universo donde la concentración de hidrógeno era mayor, éste se empezó a condensar debido a la fuerza de la gravedad, apareciendo las primeras estrellas y en su conjunto, las primeras galaxias. Aquí empezó a gestarse la inmensa fábrica de elementos que es una estrella.
Una estrella es una ingente masa de plasma (gas formado por iones y electrones a temperaturas muy altas) que se mantiene en equilibrio. Por un lado, la atracción gravitatoria haría que la estrella colapsara, pero por otro lado, la enorme presión que ejerce la estrella hacia su interior hace que la temperatura aumente hasta unos valores de millones de grados en su interior. A esa temperturas los átomos alcanzan unas velocidades enormes y al chocar entre si, se producen reacciones de fusión nuclear. En una reacción de este tipo, dos átomos se fusionan (deberíamos decir sus núcleos) y forman otro átomo distinto. Lógico, porque ha variado el número de protones del núcleo Por ejemplo, a partir del hidrógeno (protón) se puede obtener helio por el proceso denominado PP (protón-protón) y que se desarrolla en tres pasos:
1H +1H → 2H + e++ ν0
3He +3He → 24He + 21H
En
la primera reacción y durante la colisión, un
protón se convierte en un neutrón que se une al
otro
protón para formar un átomo de deuterio,
también se forma un positrón
( e+)
que es un electrón con carga positiva (es antimateria) y un
neutrino (ν0)
que es una partícula muy misteriosa y de la que se sabe muy
poco, se cree que no tiene masa y no está cargada. En la
segunda
reacción un deuterio y un protón se fusionan y dan
un
isótopo de helio ( 3He)
y finalmente, la fusión de dos átomos de este
isótopo producirían dos átomos de
helio normal (4He).
Los procesos mencionados ocurren con desprendimiento de mucha
energía
, esto explica la enorme emisión de energía de
una estrella en forma de
radiación electromagnética y consecuentemente,
calor.
212C
→23Mg + 1HEl
proceso no se detiene ahí pues a su vez el helio puede
fusionarse entre
sí para producir nuevos elementos y desprendiendo mucha
energía
.
4He + 4He → 8Be
4He + 8*Be → 12*C→ 12C + energía
Otros ejemplos de síntesis de elementos por fusión son:
212C →24Mg
.
4He + 4He → 8Be
4He + 8*Be → 12*C→ 12C + energía
Otros ejemplos de síntesis de elementos por fusión son:
212C →24Mg
212C →23Mg + n
212C →20Ne + 4He
e, incluso para átomos más pesados
216O →32S + energía
216O →31P + 1H
216O →28Si + 4He
Dependiendo de la edad de la estrella y de su masa, los procesos pueden continuar hacia metales de transición como el Fe, Co, Ni
228Si → 56Ni
56Ni → 56Co + e-
56Co → 56Fe + e-

Una galaxia es un
cúmulo de miles de millones de estrellas que estan
compuestas en un 75% por hidrógeno



La nucleosíntesis
artificial: Jugando a ser estrellas
Fue el físico inglés Rutherford el primero que consiguió fabricar un elemento químico a partir de otro. En uno de los experimentos que hizo para desentrañar la estructura del núcleo, notó que en presencia de partículas alfa (que no son otra cosa que núcleos de helio) el nitrógeno atmosférico se convertía en el isótopo 17 del oxígeno. La reacción la podemos escribir:
4He + 14N → 17O
De esta manera Rutherford abrió el camino a la nucleosíntesis artificial. El sueño de los alquimistas de transmutar la materia de manera artificial empezaba a cumplirse.
A partir de ahí se fueron estableciendo métodos para bombardear núcleos de un elemento con partículas más ligeras, por ejemplo, para producir isótopos radiactivos. La inmensa mayoría de los elementos radiactivos que se usan en medicina, la investigación o la industria se fabrican así.
Un gran problema que se encontraron los científicos para imitar a las estrellas era que, a medida que se usan núcleos más pesados, el proyectil con el que se les bombardea tiene que ir más rápido si se quiere que efectivamente se produzca la fusión. Esa "rapidez" la consigue la estrella gracias a la inmensa cantidad de energía que se desprende en los procesos descritos anteriormente y que ocasionan un aumento de la temperatura de millones de grados kelvin. En un laboratorio, eso no se puede hacer (por lo menos de momento), por eso lo que se hace es acelerar las partículas que sirven de proyectil (normalmente partículas cargadas) mediante campos electromagnéticos. A los dispositivos que producen esos proyectiles ultrarrápidos (casi la velocidad de la luz) se denominan aceleradores de partículas.
El primer acelerador de partículas especial para este tipo de colisiones fue el denominado ciclotrón. Fue construido por Lawrence, físico americano en cuyo honor se nombró al elemento 103 como laurencio, fue alrededor de 1930 en la Universidad de Berkeley (California). El abrió el camino, y a partir de ahí se hicieron aparatos que aceleraban más y más.
Fue el físico inglés Rutherford el primero que consiguió fabricar un elemento químico a partir de otro. En uno de los experimentos que hizo para desentrañar la estructura del núcleo, notó que en presencia de partículas alfa (que no son otra cosa que núcleos de helio) el nitrógeno atmosférico se convertía en el isótopo 17 del oxígeno. La reacción la podemos escribir:
4He + 14N → 17O
De esta manera Rutherford abrió el camino a la nucleosíntesis artificial. El sueño de los alquimistas de transmutar la materia de manera artificial empezaba a cumplirse.
A partir de ahí se fueron estableciendo métodos para bombardear núcleos de un elemento con partículas más ligeras, por ejemplo, para producir isótopos radiactivos. La inmensa mayoría de los elementos radiactivos que se usan en medicina, la investigación o la industria se fabrican así.
Un gran problema que se encontraron los científicos para imitar a las estrellas era que, a medida que se usan núcleos más pesados, el proyectil con el que se les bombardea tiene que ir más rápido si se quiere que efectivamente se produzca la fusión. Esa "rapidez" la consigue la estrella gracias a la inmensa cantidad de energía que se desprende en los procesos descritos anteriormente y que ocasionan un aumento de la temperatura de millones de grados kelvin. En un laboratorio, eso no se puede hacer (por lo menos de momento), por eso lo que se hace es acelerar las partículas que sirven de proyectil (normalmente partículas cargadas) mediante campos electromagnéticos. A los dispositivos que producen esos proyectiles ultrarrápidos (casi la velocidad de la luz) se denominan aceleradores de partículas.
El primer acelerador de partículas especial para este tipo de colisiones fue el denominado ciclotrón. Fue construido por Lawrence, físico americano en cuyo honor se nombró al elemento 103 como laurencio, fue alrededor de 1930 en la Universidad de Berkeley (California). El abrió el camino, y a partir de ahí se hicieron aparatos que aceleraban más y más.
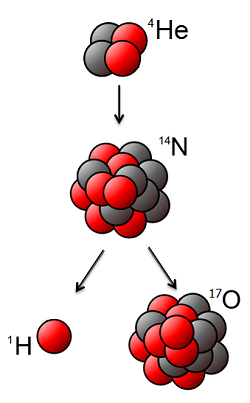
Representación de la
primera reacción de nucleosíntesis debida a
Rutherfrd

Ernest
Lawrence(1901-1958). físico americano inventor del
ciclotrón, que posibilitó el desarrollo de las
reacciones
nucleares artificiales.
El tecnecio, había sido predicho por Mendeleyev quien reservó para él un hueco en su tabla de elementos y lo llamó eka-manganeso (eka significa "debajo de"). Sin embargo, no se le encontraba por ningún lado. La razón no es otra que la inestabilidad de todos sus isótopos. Aunque se hubiera formado, en la Tierra habría desaparecido mucho tiempo atrás. Sin embargo se produce como producto residual de la fisión del uranio en reactores nucleares, esto se comprobó en 1937. Eso ha permitido estudiarlo, obtener más isótopos e incluso, actualmente se usa en la industria y en medicina. Su isótopo más estable apenas duraría unos millones de años, de ahí que en la Tierra no se encuentre, aunque si se ha detectado en estrellas del tipo "gigante roja". El nobre de tecnecio hace referencia a su carácter artificial.
Otro elemento al que vamos a hacer referencia es el prometio que era el único elemento de las tierras raras que no se había descubierto aunque, evidentemente, se sabía que debería existir. En 1944 se le detectó como producto residuo de la fisión del uranio. Se puede fabricar mediante bombardeo del 46Nd con neutrones.
Los elementos transuránidos son los elementos con Z>92 (uranio). A partir del uranio no tienen existencia en la Tierra, la razón es que todos sus isótopos son radiactivos desintegrándose en su totalidad en un tiempo bastante más pequeño que la edad de la Tierra.
El primero de la serie, el neptunio se obtuvo en 1940 al bombardear con núcleos de deuterio el uranio. El siguiente, el plutonio, se produjo por primera vez en la Universidad de Berkeley en 1940 por G. T. Seaborg y sus colaboradores bombardeando uranio 238 con neutrones. Fue también Seaborg el que obtuvo el siguiente elemento en 1944: el americio. Para ello bombardeó plutonio 239 con neutrones.
De nuevo Seaborg, en Berkeley, obtiene en 1944 el curio, bombardeando con partículas alfa el plutonio.
El mismo autor obtiene el berkelio en 1949, bombardeando curio con partículas alfa y el californio en 1958. Los nombres de berkelio y californio, hacen honor a la universidad y el estado donde está el laboratorio donde se obtuvieron estos elementos. Seaborg tuvo el honor de ver como bautizaban al elemento 106 con su nombre, seaborgio. Rarísimo honor porque normalmente estas cosas, si ocurren, lo son después de fallecido el homenajeado.
Albert Ghiorso, del equipo de Seaborg que produjo los elementos anteriores continuó con el tema y sintetizó del 99 al 103 (del Es al Lr). El einstenio se puede sintetizar a partir del curio bombardeándolo con neutrones. El fermio , bombardeando uranio 238 con iones de nitrógeno (1952). Bombardeando einstenio con partículas alfa, se obtuvo el mendelevio (1955). El nobelio se descubrió en 1966 como residuo en una explosión nuclear y finalmente el laurencio se sintetizó en 1961 bombardeando californio con núcleos de boro. Con este último se completó la familia de los actínidos.
Los transactínidos: Americanos, rusos y alemanes
Si
hasta ahora había sido el grupo de Seaborg y mas tarde el de
Ghiorso,
los que habían agregado elemento tras elemento a la Tabla
Periódica,
entró en juego otro competidor perteneciente a la ciencia
rusa (por
aquel entonces parte de la Unión Soviética) y
más concretamente, al
Instituto Conjunto para la investigación nuclear de Dubnia.
En 1964
científicos de este instituto comunicaron que
habían sintetizado el
elemento 104 al bombardear plutonio con iones de neón y
pusieron al
nuevo elemento el nombre de kurchatovio. Por otro lado, los miembros
del laboratorio de Berkeley comunicaron en 1969 que también
lo habían
sintetizado al bombardear una muestra de californio 249 con iones de
carbono 12 y al mismo tiempo negaron la vía de
síntesis propuesta por
los rusos porque al repetir el experimento no encontraron nada de lo
afirmado por ellos. Para encender más la guerra, pusieron al
elemento
el nombre rutherfordio. La disputa fue una escaramuza
más de la
denominada "guerra fría" y hasta el año
1997, la IUPAC no zanjó la cuestión
dando al elemento
104 de la Tabla Periódica su nombre actual:
rutherfordio. Algo parecido ocurrió con el el
elemento 105, los soviéticos
lo obtuvieron en 1968 bombardeando átomos de americio 243 con iones
neón 22, bautizándole con el nombre de
nielsbhorio (en honor de Niels
Bohr). Por su parte los americanos, liderados por Ghiorso en 1970,
comunican su obtención mediante el bombardeo de californio
249 con
nitrógeno 15 y para no ser menos, le dan el nombre de hahnio
(en honor
de Otto Hahn, el descubridor de la fisión nuclear). Hasta
1997 la
IUPAC, no reconoció la autoría rusa, pero dio al
elemento 105 el nombre
de dubnio, en honor a la ciudad donde reside el laboratorio ruso. Con
el elemento 106 pasó lo mismo, los americanos en 1974
comunicaron su
síntesis y los rusos en ese mismo año
también hicieron lo mismo, eso
si, variaba la forma de obtención y se consiguió
un isótopo distinto.
Los americanos propusieron el nombre de seaborgio (en honor de Seaborg,
del que ya hemos hablado) que no fue aceptado por la comunidad
internacional hasta 1997.
Con el elemento 107 aparece otro grupo de investigación, esta vez alemán, o denominado "Sociedad para la Investigación de los Iones Férricos Pesados", situado en Darmstadt (estado de Hessen) y dirigido por Peter Armbruster. En 1981 obtienen el elemento 107, llamado bohrio por la IUPAC en 1997, bombardeando bismuto 209 con iones de cromo 54. En 1984 sintetizan el elemento 108, que no recibe su nombre, hassio, hasta 1997, pues el nombre de hahnio fue rechazado al considerar que Otto Hahn había colaborado con los nazis. El 109 se obtuvo bombardeando bismuto 210 con hierro 74 y recibió en 1997 el nombre de meitnerio en honor de Lise Meitner física de origen austriaco y nacionalidad sueca que para colmo del pobre Hahn, era su discípula y colaboradora, pero en este caso se alabó el hecho de que fuera judía y por tanto perseguida por Hitler y los suyos, además de que se quedara sin Nobel por su exilio. El elemento 110, darmstadio, se sintetiza en 1994 bombardeando plomo 208 con iones de niquel 62, obteniéndose apena unos pocos átomos de él. El elemento 111, roentgenio, tambien se sintetiza en 1994 al bombardear átomos de bismuto con iones de níquel. Finalmente en 1996, se sintetiza el elemento 112, el copernicio, último elemento reconocido y nombrado por la IUPAC. Con él se completa la cuarta serie de metales de transición de la Tabla periódica.
Con el elemento 107 aparece otro grupo de investigación, esta vez alemán, o denominado "Sociedad para la Investigación de los Iones Férricos Pesados", situado en Darmstadt (estado de Hessen) y dirigido por Peter Armbruster. En 1981 obtienen el elemento 107, llamado bohrio por la IUPAC en 1997, bombardeando bismuto 209 con iones de cromo 54. En 1984 sintetizan el elemento 108, que no recibe su nombre, hassio, hasta 1997, pues el nombre de hahnio fue rechazado al considerar que Otto Hahn había colaborado con los nazis. El 109 se obtuvo bombardeando bismuto 210 con hierro 74 y recibió en 1997 el nombre de meitnerio en honor de Lise Meitner física de origen austriaco y nacionalidad sueca que para colmo del pobre Hahn, era su discípula y colaboradora, pero en este caso se alabó el hecho de que fuera judía y por tanto perseguida por Hitler y los suyos, además de que se quedara sin Nobel por su exilio. El elemento 110, darmstadio, se sintetiza en 1994 bombardeando plomo 208 con iones de niquel 62, obteniéndose apena unos pocos átomos de él. El elemento 111, roentgenio, tambien se sintetiza en 1994 al bombardear átomos de bismuto con iones de níquel. Finalmente en 1996, se sintetiza el elemento 112, el copernicio, último elemento reconocido y nombrado por la IUPAC. Con él se completa la cuarta serie de metales de transición de la Tabla periódica.

Glenn
T. Seaborg (1912-1999) científico americano,
sintetizó
varios elementos actínidos y fue uno de
los padres
de la Tabla Periódica actual. Premio Nobel de
Química en 1951. En su honor , el elemento 106 de
la
tabla periódica lleva su nombre.


Albert Ghiorso
(1915-2010), científico americano codescubridor con Seaborg
de
varios elementos y también como director del
laboratorio
de Berkeley . En total descubrió 12 elementos, del 95 al 106.


Lise Meitner
(1878-1968), científica sueca de origen austriaco, codescubridora de la fusión nuclear.

Wilhem
Röentgen (1845-1923) científico alemán
descubridor de los rayos X.

Los
elementos transactínidos son muy
inestables y se desintegran rápidamente, por
ejemplo el copernicio tiene
una vida media de 0,25 milisegundos. Esto hace que solamente la
curiosidad científica mantenga la
investigación en este terreno, ya que
la aplicación industrial o cientifica es nula. En su
momento, Seaborg
postuló que alguno de éstos elementos
tendrían una estabilidad mayor,
pero tal extremo no se ha confirmado y, en general, a medida que
aumenta el número atómico tambien disminuye la
vida media del elemento.
Más allá...
Aunque
la IUPAC todavía no les ha reconocido nombre, existen
suficientes
evidencias de que se han sintetizado del 113 al 118. De momento reciben
nombres en latín que solamente significa su
número, por ejemplo
ununtrio sería la denominación del elemento 113.
A los elementos del 113 al 118 se les conoce como átomos superpesados, su inestabilidad es todavía mayor y solamente se han detectado unos pocos átomos de cada uno de ellos.
La pregunta que nos formulamos es ¿Hasta cuándo se seguirán sintetizando nuevos elementos? La respuesta no es sencilla. Parece que con los últimos elementos se ha llegado casi hasta el límite actual de la técnica. Los elementos son cada vez más inestables y se obtienen apenas unos átomos, pero por otro lado, los aceleradores de partículas y los instrumentos de detección mejoran cada vez más, luego ¿quién sabe?...